https://legkovmeste.ru/
http://megapoisk.com/
https://sovets24.ru/
https://melscience.com/RU-ru/chemistry/
https://ru.wikipedia.org/wiki/Сульфат_никеля
https://chem. ru/acetat-kobalta-ii.html
https://kristallov.net/metodica.html
Pokusy v domácí laboratoři – M.: Nauka. Hlavní redakce fyzikální a matematické literatury, 1980, 144 s.
Svět chemie. Zábavné příběhy o chemii. Petrohrad. “Mime Express” 1995
Úvod
Krystaly hrály a stále hrají důležitou roli v přírodě i v životě člověka. Téměř všechny horniny jsou složeny z různých krystalů. Pouze malý počet z nich má složení odpovídající čisté látce, protože v přírodě se všechny látky neustále mísí pod vlivem větru, vody a dalších faktorů.
Minulý rok jsem připravil projekt, ve kterém jsem v laboratoři pěstoval krystaly z čistých solí. Podařilo se mi vypěstovat úžasně krásné krystaly. Lišily se barvou, tvarem, křehkostí a rychlostí tvorby. Opravdu mě bavilo pěstovat krystaly, sledovat, jak rostou, a přemýšlel jsem: získali byste krystaly, kdybyste smíchali různé soli? Jaký tvar a barvu takové krystaly vyrostou?
Toto téma mě velmi zaujalo a ve svém novém výzkumu jsem si stanovil za cíl vypěstovat krystaly ze směsi dvou solí. Moje hypotéza: za stejných podmínek růstu rostou z různých solí krystaly různých barev, tvarů a velikostí. A když se smíchají různé soli, některé z nich spolu reagují a dávají novou krystalickou formu a některé ne.
K dosažení tohoto cíle jsem si stanovil následující úkoly:
· vyhledat a prostudovat si v literatuře informace o krystalech, o směsi krystalů, o pěstování krystalů ze soli v laboratoři nebo doma;
· prostudovat potřebná bezpečnostní opatření a dodržovat je při provádění experimentu;
· vybrat zařízení a sůl pro pěstování krystalů ve školní laboratoři;
· vypěstovat krystaly ze směsi dvou solí, z nichž jedna je kuchyňská sůl;
· prozkoumat je, popsat jejich tvar, vyfotografovat je;
· analyzovat získané výsledky a vyvodit závěry.
Jako předměty výzkumu jsem si vzal krystaly směsi dvou solí a jako předmět výzkumu jsem si vzal krystalizační proces.
Praktický význam mé práce: nabyté dovednosti a schopnosti lze využít v hodinách o okolním světě, v mimoškolních aktivitách, výsledná malá sbírka může sloužit jako názorná pomůcka.
Stručné informace o krystalech.
Krystaly (z řeckého κρ?σταλλος původně – “led”, později – “horský krystal; krystal”) jsou pevná tělesa, ve kterých jsou částice (atomy a molekuly) uspořádány pravidelně a tvoří trojrozměrné periodické prostorové uspořádání – krystalovou mřížku. .
Krystaly jsou v přírodě běžné a lze je získat i v laboratoři. Například sněhové vločky, mrazivé vzory na okenním skle a námraza, která v zimě zdobí holé větve stromů.
Většina přírodních krystalů má hladké hrany; Okraje krystalů jsou opticky ploché a obvykle poskytují jasné odlesky okolí (jako u okenního skla). Ploché plochy krystalů naznačují správné vnitřní uspořádání atomů.
Krystaly, které se nacházejí v přírodě, nejsou čistou látkou a obsahují různé nečistoty, které mohou snížit symetrii krystalové mřížky, způsobit drsné hrany, krystal nemusí mít správný tvar: krystal bude neprůhledný nebo omezeně průhledný. U přírodních krystalů jsou odlesky více rozmazané, a proto samotné tváře nejsou dokonale ploché. Podmínky, ve kterých krystaly rostou, jsou rozhodující pro formu, ve které se tvoří. Faktory, jako jsou teplotní změny a blízké okolí se sousedními pevnými látkami, někdy brání rostoucímu krystalu v získání jeho charakteristického tvaru.
Významným mezníkem v dějinách krystalografie byla kniha napsaná v roce 1784 francouzským opatem R. Gaüyem. Předpokládal, že krystaly vznikají správným uspořádáním malých identických částic, které nazval „molekulární bloky“. Haüy ukázal, jak lze položením takových „cihel“ získat hladké, ploché okraje kalcitu. Přibližný mechanismus růstu krystalů lze znázornit ve formě diagramu, který je znázorněn na obrázku 1.
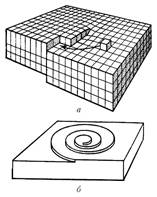
Obrázek 1. Schémata růstu krystalů: a) skládání „molekulárních bloků“, b) spirálovitý růst krystalů.
Jsou-li v roztoku přítomny dvě soli současně, mohou spolu reagovat za vzniku slabě rozpustné látky. Pak jeho krystaly, vypadnoucí z roztoku, vytvoří rostoucí krystal jiného tvaru než krystaly soli, které byly původně rozpuštěny Zvláštnosti rostoucích krystalů.
Mohou růst jak v přírodě, tak v umělých podmínkách. Ve slaných jezerech, v mělkých mořích a zálivech se voda ohřívá a odpařuje. Sůl rozpuštěná ve vodě se sráží, usazuje se na dně, na kamenech atd. Tak vznikají slaniska, nejčastěji dna vyschlých jezer.
V umělých podmínkách se krystaly pěstují z roztoku nebo z taveniny. Experimenty s pěstováním umělých krystalů začaly ve starověku, od dob alchymistů. Zpočátku sledovali jiné cíle: získání kamene mudrců, obohacení, získání ideálního krystalu a tak dále.
Zvláštnosti pěstování krystalů v laboratoři jsou založeny na tom, že soli mají různou rozpustnost a tento index rozpustnosti se mění se změnami teploty (s poklesem teploty rozpustnost klesá a se stoupající teplotou se rozpustnost zvyšuje). Například síran měďnatý (CuSO4) lze rozpustit při 30 stupních pouze asi 25 g na 100 ml vody, ale pokud se teplota zvýší na 80 stupňů, jeho rozpustnost se zvýší na asi 55 g na 100 ml.
Ke krystalizaci soli dochází vlivem poklesu teploty, protože se snižuje rozpustnost soli. Ke krystalizaci dochází také v důsledku odpařování vody ze solného roztoku. Ukazuje se, že není dostatek vody, ve které je rozpuštěna, aby se sůl rozpustila, a proto se sůl usadí na dně sklenice nebo jinými slovy krystalizuje.
Postup při provádění experimentu.
Všechny fáze mého experimentu doprovázeli dospělí – vedoucí mého projektu Makarenkova G.Yu., a při domácím pěstování krystalů – moje matka Alena. Pomáhali mi a dohlíželi na mě v některých procesech. Při provádění experimentů jsem přísně dodržoval bezpečnostní pravidla.
Pro pěstování krystalů jsem vzal barevné soli (názvy uvedu níže) a rozpustil je napůl kuchyňskou solí (podle hmotnosti). Všechny hmotnosti byly měřeny pomocí laboratorních elektronických vah a množství vody bylo přibližně měřeno pomocí značek na chemických kádinkách.
Všechny krystaly byly pěstovány za stejných podmínek, aby bylo zajištěno, že tvar krystalů nezávisí na experimentálních podmínkách.
Postupoval jsem podle následujícího postupu:
· Vezměte čisté nádobí – skleněné kádinky o objemu 150-200 ml a plastové nádoby o objemu 300-500 ml;
· Do kádinky nasypte 10 g soli, do stejné sklenice přidejte 10 g kuchyňské soli;
· S pomocí dospělého přidávejte horkou, nejlépe vroucí vodu (aby se co nejvíce soli rozpustilo), sůl míchejte skleněnou tyčinkou do úplného rozpuštění;
· Po troškách přidávejte směs soli (sůl a kuchyňská sůl) v poměru 1:1, občas zamíchejte a sůl sekejte tyčí, dokud se nepřestane rozpouštět v horké vodě;
· Na dno čisté plastové nádoby položte čisté kameny, horký roztok z kádinky s pomocí dospělých přelijte do plastové nádoby;
· Nechte po dlouhou dobu krystalizovat a soli se začnou usazovat na stěnách, dně a zavedených oblázcích ve formě malých krystalů;
· Vyjměte hotové krystaly z roztoku pomocí pinzety a osušte ubrousky;
· Prohlédněte si lupou a pořiďte fotografii;
· Porovnejte s výsledky mého předchozího projektu.
Velmi důležité detaily, kterým je třeba věnovat pozornost:
· Experimentální náčiní musí být čisté. Solný roztok se připravuje přesně ve stanoveném poměru.
· Čím vyšší je teplota vody, tím rychleji se v ní rozpouštějí soli.
· Musíte okamžitě určit místo, kde může nádoba s roztokem bezpečně stát po dlouhou dobu. Toto místo by také mělo být daleko od baterie.
· Musíme být trpěliví. Krystalizace je dlouhý proces, který trvá několik dní až dva až tři týdny.
· Když křišťál vyroste, můžete jej přetřít lakem – ochrání výrobek před bílými usazeninami při skladování a dodá mu lesk.
K pěstování krystalů jsem použil následující soli:
· octan měďnatý nebo octan měďnatý (Cu(CH3COO)2);
· síran měďnatý nebo síran měďnatý (CuSO4);
· síran nikelnatý nebo síran nikelnatý (NiSO4);
· soda vápenatá nebo uhličitan draselný (K2CO3);
· octan kobaltnatý nebo octan kobaltnatý (Co(CH3COO)2);
· dusičnan amonný (NH4NO3);
· jodid draselný nebo jodid draselný (KI);
· železitoamonný kamenec NH12Fe(SO?)? XNUMXHXNUMXO.
Ke všem solím jsem přidal kuchyňskou sůl nebo chlorid sodný (NaCl), hmotnosti byly stejné – po 10 g soli a kuchyňské soli. Podařilo se mi vypěstovat úžasně krásné krystaly.
Růst krystalů na horninovém podkladu ve všech roztocích začal přibližně po dvou až třech dnech. Po týdnu je bylo možné vyšetřit a dokonce pomocí pinzety vyjmout z roztoku. Krystaly jsme prakticky nerušili, nádobami nehýbali, abychom nenarušili růst krystalů. Krystaly se zvětšovaly, jak se voda odpařovala.
Krystaly rostly nejen na kamenném podstavci, ale i na stěnách nádoby a na dně. Růst krystalů se zastavil, až když se všechna voda odpařila. Poté jsme vyfotografovali výsledné krystaly.
Roztoky, které jsme nechali pro krystalizaci, jsou uvedeny na obrázku 2.
Obrázek 2. Připravené roztoky byly ponechány krystalizovat.
Fotografie narostlých krystalů, které jsme pořídili během experimentu, jsou uvedeny na obrázcích níže. Fotografie některých krystalů jsou uvedeny v porovnání s krystaly čisté hmoty, které jsem vypěstoval minulý rok.
Octan měďnatý a Octan měďnatý a kuchyňská sůl.
Fotografie hotových krystalů jsou uvedeny na obrázcích 3-5. Při zkoumání krystalů jsme si všimli, že krystaly čisté látky mají správný tvar, jsou také pevné, tmavě modrozelené barvy, některé jsou průsvitné. Krystaly vyrostlé ze směsi solí svým tvarem připomínají korály nebo mraky. Na fotografii 5 jsou vidět krystaly kuchyňské soli a octanu sodného, tónované octanem měďnatým, také samostatně (hlavně dole) krychlové krystaly kuchyňské soli a jednotlivé krystaly octanu měďnatého (tmavé inkluzní krystaly).
Síran nikelnatý nebo síran nikelnatý.
Krystal neroste tak rychle jako jiné soli, má tmavší barvu a tvar komolého jehlanu. Fotografie hotových krystalů jsou uvedeny na obrázcích 6-7.


Obrázek 3. Výsledné různé krystaly octanu měďnatého v nádobě, na dně, stěnách a kamenné základně.
Obrázek 4. Detail monokrystalů octanu měďnatého.
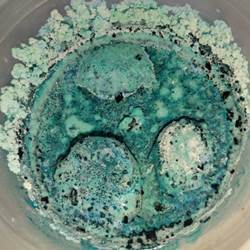
Obrázek 5. Různé krystaly získané ze směsi solí octanu měďnatého a kuchyňské soli v nádobě, na dně, stěnách a kamenném podstavci.
Lze poznamenat, že krystaly čisté látky jsou zřetelně jehličkovité, zatímco tvar krystalů ze směsi solí má hrany vyhlazené, zaoblený tvar, jakoby natavené hrany. Dochází k barevnému přechodu (tónované krystaly). S největší pravděpodobností z roztoku také vypadly krystaly síranu sodného a chloridu nikelnatého.

Obrázek 6. Krystaly síranu nikelnatého (loňský projekt).
Obrázek 7. Různé krystaly získané ze směsi síranu nikelnatého a kuchyňské soli v nádobě, na dně, stěnách a kamenném podstavci.
Soda a kuchyňská sůl.
Krystaly čisté sody se ukázaly být nestabilní, křehké, pokryté bílým povlakem a zničené. Krystaly solné směsi se ukázaly být odolnější. Vypadají jako bílé mraky. Na dně nádoby ve směsi solí jsou vidět i jednotlivé krystalky kuchyňské soli – jsou krychlového tvaru. Fotografie jsou uvedeny na obrázcích 8-9.

Obrázek 8. Krystaly sody (loňský projekt).
Obrázek 9. Různé krystaly získané ze směsi sodných solí a kuchyňské soli v nádobě, na dně, stěnách a kamenném podstavci.
Jodid draselný a kuchyňská sůl. a dusičnan amonný a kuchyňská sůl.
Tyto dva experimenty se nezdařily, protože nebylo možné získat žádné velké izolované krystaly. Sůl se usadila ve formě nažloutlého a bílo-krémového filmu na dně, kamenném podstavci a stěnách nádoby. Krystaly jsou velmi malé, těžko rozlišitelné a nenápadné. Je vidět barevný přechod, krystaly různých tvarů.
Kamenec železnatý amonný a kuchyňská sůl.
Při přípravě roztoku této soli spolu s kuchyňskou solí se roztok zakalil a myslel jsem si, že z toho nic nebude, ale přesto jsem to nechal na krystalizaci. S největší pravděpodobností došlo k výměnné reakci mezi látkami v roztoku a v důsledku toho rostly společně krystaly kuchyňské soli, síranu amonného, chloridu amonného, síranu železnatého a síranu sodného.
Fotografie hotových krystalů je na obrázku 10.
Síran měďnatý a kuchyňská sůl.
Roztok čistého modrého síranu měďnatého. Když se směs solí (s kuchyňskou solí) rozpustí, získá světle zelenou barvu. Při odpařování vody vznikají neobvyklé světle zelené krystaly neobvyklého tvaru, podobné zeleným keřům. Přesně jak je popsáno výše, dochází k výměnné reakci a rostou krystaly čtyř různých solí: síran měďnatý, síran sodný, chlorid sodný a chlorid měďnatý. Fotografie krystalů jsou uvedeny na obrázku 11-13.

Obrázek 10. Krystaly ze směsi železito-amonných kamencových solí a kuchyňské soli.
Obrázek 11. Krystaly síranu měďnatého (loňský projekt).


Obrázek 12. Krystaly směsi různých solí, podobné zeleným keřům.
Obrázek 13. Krystaly ze směsi síranu měďnatého a kuchyňské soli (směs různých krystalů).
Octan kobaltnatý a kuchyňská sůl.
Ukázalo se, že roztok má tmavě růžovou barvu. Krystaly ze směsi s kuchyňskou solí vyrostly jako tmavě růžové řasy. Můžete si všimnout jednotlivých krystalů kuchyňské soli (průhledné malé kostičky) a malých jehličkovitých krystalů octanu kobaltnatého. Fotografie krystalů jsou uvedeny na obrázcích 14-15.

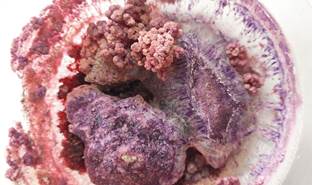
Obrázek 14. Krystaly octanu kobaltnatého (loňský projekt).
Obrázek 15. Krystaly ze směsi solí octanu kobaltnatého a kuchyňské soli. Jsou vidět krystaly různých tvarů
Závěry na základě výsledků práce.
Při experimentech jsem dospěl k následujícím závěrům:
· Krystal lze pěstovat pomocí nasyceného roztoku soli;
· Horká voda je schopna rozpustit více soli, takže při ochlazení sůl, která se nemůže rozpustit, vypadne z roztoku a začne tvořit krystal;
· Aby se krystal mohl začít tvořit, je nutná platforma nebo povrch. Použil jsem kameny, ale ve většině případů krystaly rostly i po stranách nádob;
· Krystaly rostou v různých časech;
· Různé soli tvoří krystaly, i když rostou za stejných podmínek;
· Soli, jsou-li smíchány mezi sebou, jsou schopny tvořit krystaly různých tvarů, které rostou jak společně, tak paralelně, vedle sebe;
· Krystaly vyrostlé ze směsi solí, nejčastěji tvarově nepodobné krystalům stejných solí v jejich čisté formě;
· V solných roztocích často dochází k výměnným reakcím a místo dvou solí se při krystalizaci tvoří čtyři různé soli;
· Barevné soli mohou zabarvit průhledné krystaly kuchyňské soli nebo bílé soli síranu sodného a vytvořit tak různé odstíny a barevné přechody (rozostření barev);
· Krystaly čisté hmoty se vyznačují úžasnou pravidelností a přesností struktury, identické v každé její části. Zatímco krystaly solné směsi tvoří bizarní tvary, vypadají jako živé rostliny nebo korály a mají duhové barvy;
· Krystaly jsou velmi krásné, fascinují, chci je držet v rukou, dívat se na ně donekonečna a zdá se, že umím vytvářet krásu.
Závěr.
Přírodní krystaly vždy vzbuzovaly mezi lidmi zvědavost. S krystaly byly spojeny různé pověry. Později, když se stejné minerály začaly brousit a leštit jako drahé kameny, se u „šťastných“ talismanů a „vlastních kamenů“ odpovídajících měsíci narození uchovalo mnoho pověr.
Dnes našly krystaly kromě svůdných vlastností velmi široké uplatnění ve vědě a technice: polovodiče, hranoly a čočky pro optická zařízení, pevnolátkové lasery, optické a elektrooptické krystaly, feromagnety a ferity, monokrystaly vysoce čisté kovy a další.
Horniny naší země jsou tvořeny krystaly různých solí a jejich směsí. Protože v přírodě prakticky neexistuje žádná čistá látka, tak či onak různé krystaly obsahují nečistoty a tvoří se společně. Velmi běžnou solí na zemi je chlorid sodný nebo kuchyňská sůl. Začalo mě zajímat, jak by se změnil tvar krystalu, kdyby se do směsi dostala kuchyňská sůl při jeho vzniku. Budou krystaly různých solí růst nezávisle na sobě nebo spolu vytvoří jeden krystal?
Při své práci jsem ze směsí různých solí s kuchyňskou solí vypěstoval krystaly různých tvarů a barev a objevil tento nádherný svět krystalů. Podíval jsem se, jak krystaly rostou v přírodě a jak si je můžete vypěstovat ve školní laboratoři nebo doma. Změnou druhů soli pro kultivaci lze získat krystaly různých tvarů, což bylo experimentálně potvrzeno.
















